北京2017年5月4日电 /美通社/ -- 创建于中国-新加坡苏州工业园区生物纳米园(Suzhou-SIP Biobay)、致力于具全球自主知识产权的创新单抗药物研究与产业化的生物制药企业苏州思坦维生物技术有限责任公司 (简称思坦维或Stainwei)日前获悉:该公司已进入临床研究阶段、全新的抗肿瘤血管增生(抗VEGF)单抗药物(代号hPV19)日前已正式获得美国专利商标局(USPTO)颁发的专利授权证书(专利号:US9,580,498),该专利的有效期截至2032年。这也是公司该单抗继2015年、2016年先后获中国国家知识产权局颁发两项专利授权证书之后,在单抗药物领域全球专利申请与战略布局中取得的又一重要里程碑事件。 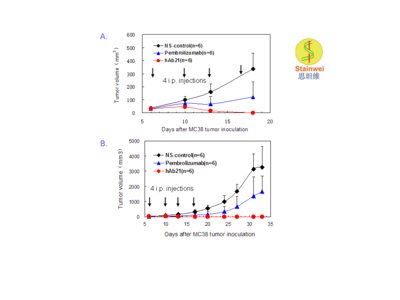 抗PD-1 单抗hAb21在PD-1人源化小鼠移植肿瘤模型中测试结果 PD-1基因人源化纯合子小鼠(基因背景为C57BL/6) 背部皮下接种数量约为1 x106的同源的小鼠结肠癌细胞MC38,待接种的肿瘤体积长至米粒大小时(约50mm3,接种后第6天),将动物随机分为3组(每组6只),分别在接种后第6, 10, 13及 17 天腹腔注射200 ug抗PD-1单抗pembrolizumab, hAb21 单抗或生理盐水。其中图A为接种肿瘤的生长早期曲线; 图B为接种肿瘤的生长全程曲线。
思坦维在研的VEGF单抗不但具有全新的氨基酸序列及独特的抗原识别位点(epitope), 且体内外生物活性比全球首个也是目前唯一获美国FDA批准上市的VEGF单抗药物Avastin (商标名:Beavacizmab Roche/Genentech公司的重磅炸弹级产品,2015年全球年销售额67亿美元)强6-8倍。 据公司负责人及该专利主要发明者之一周群敏博士介绍:“在临床前动物研究及目前在肿瘤患者中开展的I期临床研究中,hPV19单抗表现有很好的安全性/耐受性与初步疗效。” 周群敏博士还表示:“凭其独特的抗原识别表位、良好的安全性/耐受性及优于同类已上市药物(Avastin)的生物活性, hPV19 单抗药物如今后最终通过临床研究成功开发上市,其意义不但可为国内外众多肿瘤患者提供新一代的抗肿瘤血管增生药物;未来临床上还有望用于Avastin或其生物仿制药治疗无效或产生耐药的患者,进一步开拓抗血管增生药物的适应症与国内外市场。” 思坦维公司在hPV19单抗基础上还开发出一眼用生物制品新剂型药物,拟用于治疗老年黄斑变性(age-related macular degeneration,AMD)及糖尿病性黄斑水肿等与血管增生/渗透相关的致盲性眼底病,目前该项目已申请专利,临床前各项研究已完成,在申报临床批件中。 除抗血管增生VEGF单抗药物之外, 思坦维公司目前在研的另一重大项目是以通过调动机体自身免疫功能来直接攻击或杀灭肿瘤为目的抗PD-1单抗药物。思坦维公司已成功获得一代号为hAb21、全新的抗人PD-1单抗(人源化IgG4-kappa 型)。hAb21单抗结合PD-1抗原的区域/结合位点(epitope)既不同于美国Merck公司已上市的Keytruda (通用名:Pembrolizumab),也不同于美国Bristol-Myers Squibb 公司已上市的Opdivo(通用名:Nivolumab)。 更惊奇的及更具临床价值与产业化意义的是思坦维公司的hAb21单抗在PD-1人源化小鼠测试中,其抗肿瘤效果远好于同类药物Pembrolizumab。如图所示,所有接受了hAb21单抗治疗的动物在给药7-10天后,肿瘤全部出现萎缩或彻底消失,在完成第4次给药(也是最后一次给药)后停药30天以上,肿瘤也无恢复生长;而6只接受了Pembrolizumab治疗的小鼠,仅有1只(16%)动物肿瘤出现萎缩或彻底消失;其余5只在停药后7-10天,肿瘤大多又都恢复生长并很快导致动物死亡或安乐死。先前接受过hAb21单抗治疗的小鼠在第30天再重新接种MC38肿瘤 (无进一步给药),肿瘤相继在接种后10-14天内又都被彻底排斥;这批小鼠目前已第三次接种MC38肿瘤,各测试动物都依然健康存活(研究还在继续进行与观察中)。 基于这些令人鼓舞的结果,思坦维已经提交了有关hAb21单抗的专利保护申请,目前正围绕临床批件的申报在开展各项研究,计划将在2017年底向中国CFDA及美国FDA提交资料申报临床批件。 本站文章部分内容转载自互联网,供读者交流和学习,如有涉及作者版权问题请及时与我们联系,以便更正或删除。感谢所有提供信息材料的网站,并欢迎各类媒体与我们进行文章共享合作。
|
|||||||
